إستر مقابل الأثير

المحتوى
استير والأثير جزيئات عضوية مع ذرات الأكسجين. كلاهما له صلة الأثير وهو -O-. استرات لديها المجموعة -COO. ترتبط إحدى ذرات الأكسجين بالكربون مع رابطة مزدوجة ، والأكسجين الآخر مرتبط برابطة واحدة. نظرًا لأن ثلاث ذرات فقط متصلة بذرة الكربون ، فلديها هندسة مستوية مثلثية حولها. علاوة على ذلك ، ذرة الكربون هي sp2المهجنة.
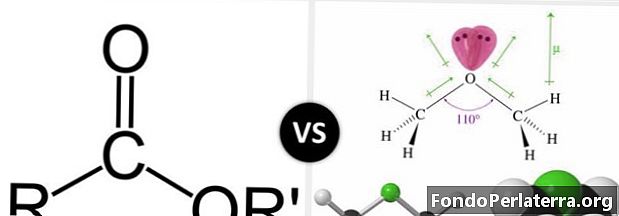
مجموعة الكربوكسيل هي مجموعة وظيفية تحدث على نطاق واسع في الكيمياء والكيمياء الحيوية. هذه المجموعة هي أصل مجموعة المركبات ذات الصلة المعروفة باسم مركبات الأسيل. تُعرف مركبات الأسيل أيضًا بمشتقات حمض الكربوكسيل. استر هو مشتق من حمض الكربوكسيل من هذا القبيل. يمتلك إستر المركب رابطة من الكربون - الكربونيل - الأكسجين ، بينما يحتوي مركب الأثير على رابطة الكربون - الأكسجين - الكربون.
المحتويات: الفرق بين إستر والأثير
- ما هو استر؟
- ما هو الأثير؟
- الاختلافات الرئيسية
- شرح الفيديو
ما هو استر؟
استرات لديها صيغة عامة ل RCOOR '. تصنع الإسترات عن طريق التفاعل بين حمض الكربوكسيل مع الكحول. تتم تسمية استرات من خلال كتابة أسماء الكحول المستمدة الجزء الأول. ثم يتم كتابة الاسم المشتق من الجزء الحمضي مع النهاية -أكل أو -oate.

ما هو الأثير؟
الأثيرون لديهم المجموعة الوظيفية ROR على سبيل المثال Ethoxypropane. الأثير هو مركب يحتوي على رابطة الكربون الأكسجين. يمكن أن تنتج الإيثرات عن طريق تجفيف الكحول بين الجزيئات. يحدث هذا عادة عند درجة حرارة أقل من الجفاف إلى الألكين.

الاختلافات الرئيسية
- استرات هي مشتقات حمض الكربوكسيل ولها مجموعة -COO. الأثيرات لديهم مجموعة وظيفية -O.
- لدى إستر مجموعة كربونية متاخمة للأكسجين ، لكن الأثير ليس كذلك.
- استرات لها الكثير من الروائح المميزة.
- يتم تحلل الإسترات بسهولة لإنتاج الكحول وحمض الكربوكسيل على عكس الإيثرات.
- لدى Esters المجموعة الوظيفية RCOOR مع رابطة C مزدوجة إلى أحد Os ورابطة واحدة إلى O على سبيل المثال إيثيل إيثانوات. في حين أن Ethers لديها المجموعة الوظيفية ROR مثل Ethoxypropane
- الأثير هو مركب يحتوي على رابطة الكربون الأكسجين. مثال على الأثير هو إيثوكسيلات. المركب الموجود أدناه هو لوريث 5. الأستر ، من ناحية أخرى ، هو مركب يحتوي على رابطة كربون كربونية - أوكسجين.
- السمة الأساسية التي تميز استر عن الأثير هي بنية مختلفة. يحتوي المركب المعروف باسم استر على رابطة الكربون - الكربونيل - الأكسجين ، في حين أن مركب الأثير لديه رابطة الكربون الكربون الأكسجين.
- الاسترات عبارة عن مركبات قطبية ، لكنها لا تملك القدرة على تكوين روابط هيدروجينية قوية مع بعضها البعض بسبب نقص الهيدروجين المرتبط بالأكسجين. نتيجة لذلك ، يكون لدى الأسترات نقاط غليان أقل مقارنة بالأحماض أو الكحوليات ذات الأوزان الجزيئية المماثلة. يمكن أن تنتج الإيثرات عن طريق تجفيف الكحول بين الجزيئات. يحدث هذا عادة عند درجة حرارة أقل من الجفاف إلى الألكين. تخليق ويليامسون هو طريقة أخرى لإنتاج إثيرات غير متماثلة.